近年来,mRNA药物作为一种新兴的治疗手段,在癌症免疫治疗、疫苗、蛋白质替代治疗以及基因治疗等领域受到了越来越多的关注。当前,RNA疗法主要依赖于脂质纳米颗粒(LNPs)进行递送,且RNA只有在封装于LNPs内时才具有药物活性,这使得研究人员难以在短时间内分析多种类型的RNA分子。而且LNP装载的RNA药物通常需要在-20 ℃或-70 ℃下进行冷链运输,成本高昂,极大地限制了这些药物在偏远地区的应用。鉴于LNP递送模式的制备过程耗时且储存和运输要求严格等局限,因此,发展一种小规模、便捷且效果优异的mRNA递送体系至关重要。
近日,刘小龙研究团队在Chemical Engineering Journal期刊 (IF=13.3) 发表研究论文“A ready-to-use RNA delivery platform modulated by metal ions”。该研究旨在利用金属离子调控脂质体的物化特性,开发出一种小批量、易于存储、即混即用的mRNA递送平台。降低成本并延长保质期,从而为新型mRNA载体的发展奠定基础。通过这一创新,希望可以实现mRNA药物的更广泛应用,为生物小分子药物和抗体药物的替代和拓展提供更多可能性,推动生物医药领域的发展。

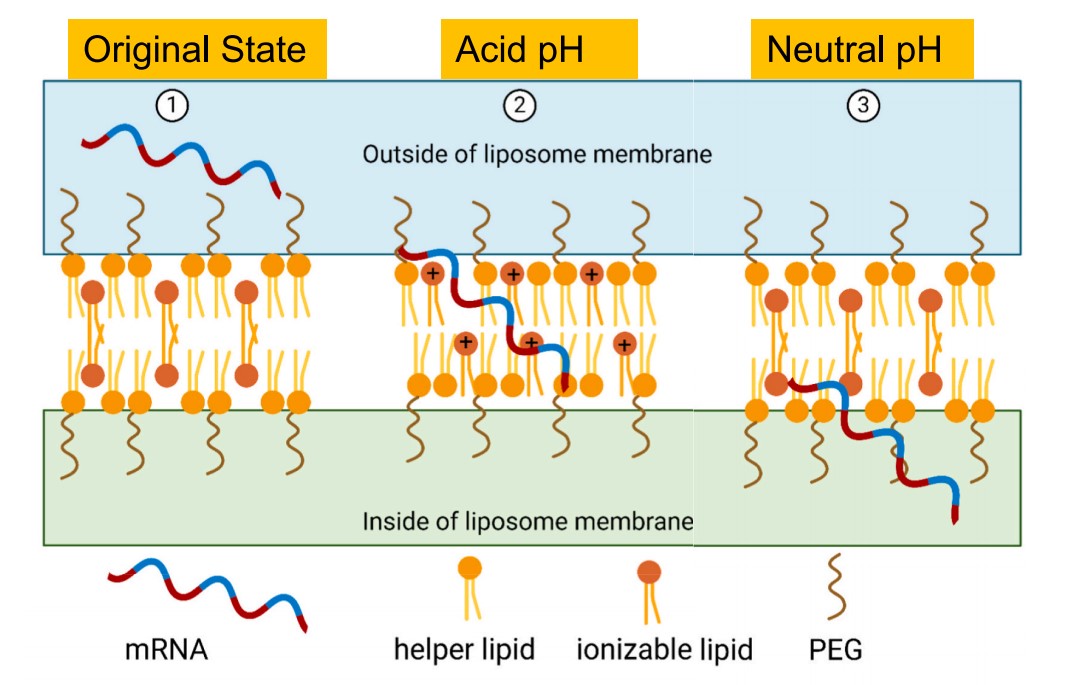
相比较于LNP,该研究提出了一种即混即用型的mRNA递送模式,该模式基于加入金属离子修饰的空载脂质体,尤其是Zn2+,可以增加RNA的装载(约1.5~2倍)和蛋白质表达(约3~7倍)。在分子尺度上,Zn2+可以重新编程脂膜的结构,最终形成更厚、更硬的脂膜,并具有更高的玻璃化转变温度。这种即混即用型的mRNA递送模式在酸性pH环境下,可电离脂质会发生质子化,并通过静电作用主动吸附mRNA。当pH值恢复至中性时,原有的静电作用力将减弱,使得mRNA能够利用介孔结构的虹吸效应以及亲疏水相互作用,顺利透过可电离脂质。在此基础上,研究团队证实了金属离子的引入能够显著提高mRNA的装载能力和表达效率,同时延长空载体的使用寿命。与传统的脂质纳米颗粒(LNP)相比,这种即用型给药策略在储存方面要求更为简单(室温或4 ℃条件下保存),且展现出更高的稳定性和体内递送效果。总的来说,这种简易且通用的RNA递送载体适用于多种不同的应用场景,展现了广阔的潜在应用前景。
该工作得到了国家自然基金、杭高院自主立项交叉项目、自主部署科研项目,杭高院启动经费和工作室经费的支持。助理研究员秦肇建、2022级硕士姜泳卓、助理研究员陶鹏为本研究的共同第一作者,刘小龙研究员为通讯作者,国科大杭州高等研究院生命与健康科学学院为第一单位。