设计和发展结构特征新颖的手性膦配体对于发现新反应、提高现有反应的效率和实用性具有十分重要的意义。汤文军实验室长期致力于P-手性膦配体的研究,在过去数年中设计和发展了一系列结构独特、具有重要应用价值的单齿和双齿膦配体,并广泛应用于不对称偶联和氢化等反应中。其中八十余个配体已经在国内外著名试剂公司Strem、Aldrich和大赛璐等销售,部分配体已经以公斤级规模应用于药物和农药生产中(Aldrichimica Acta 2020,53, 27-35)。最近,实验室在手性膦配体促进的高效不对称偶联反应中取得系列进展。
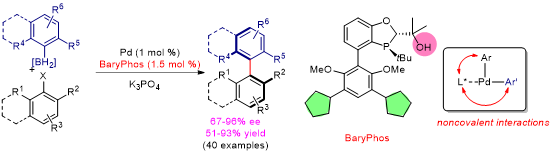
在构建轴手性邻位四取代联芳基结构方面,汤文军研究团队通过发展新型的手性单膦配体BaryPhos,成功解决了长期以来大位阻不对称Suzuki-Miyaura偶联反应中存在的活性和选择性问题,提出利用手性单膦配体分别和两个偶联底物间的非共价键相互作用有效控制对映选择性的不对称偶联新模式,发展了一个对映选择性高、底物适用性广、实用性强的不对称Suzuki-Miyaura偶联反应,高效合成了一系列轴手性邻位四取代联苯基和联萘基结构,并实现了男性避孕药及抗肿瘤药物棉酚的首次对映选择性合成。该研究工作将极大促进轴手性邻位四取代联芳基类化合物的新药研发和创制。(J. Am. Chem. Soc. 2020,142, 8036-8043)。
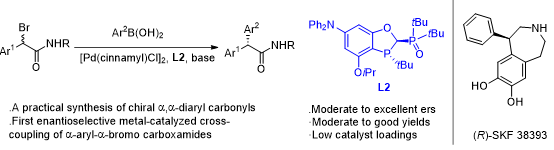
在构建手性α, α-二芳基酰胺结构方面,研究团队前期发现大位阻P,P=O配体可以有效抑制二次转金属,并首次成功实现了α-烷基-α-溴代酰胺与芳基硼酸间的钯催化不对称交叉偶联(Angew. Chem. Int. Ed.2019, 58, 11355-11359)。最近,实验室又利用手性大位阻P,P=O配体实现了钯催化α-芳基-α-溴代酰胺与芳基硼酸的不对称交叉偶联反应,首次发展了一个底物适用范围广、高效又实用的合成手性α, α-二芳基酰胺结构的方法(Org. Lett. 2020, doi.org/10.1021/acs.orglett.0c01489.)。
在构建手性螺环结构方面,课题组通过发展一个大位阻手性单膦配体高立体选择性地实现了分子内不对称α-芳基化反应,以良好到优异的收率和对映选择性实现了一系列苯并[4.4],[4.5],[4.6]螺环结构的合成,并成功应用于(-)-Cannabispirenone A和B关键中间体的合成中。(Org. Lett. 2020, doi/10.1021/acs.orglett.0c01129.)。

在构建手性杂环方面,课题组利用手性双膦配体WingPhos,发展了一个钯催化不对称串联烯丙基二取代反应,高对映选择性地实现了系列乙烯基取代的四氢喹喔啉、哌嗪、二氢苯并噁嗪和吗啉结构。该反应具有优秀的产率、区域选择性和对映选择性,催化剂当量最低可至0.1 mol%(Org. Lett. 2020, doi/10.1021/acs.orglett.0c01490.)。

在构筑桥环手性季碳结构方面,课题组最近发展了一个高效的钯催化去芳构环化反应,能有效构建多种环尺寸或杂环的含季碳桥联四环骨架。该方法底物适用性广,可以用于众多天然产物骨架的简易合成。值得注意的是,在一个手性钯催化剂作用下,利用去对称化策略通过一个不对称去芳构环化反应可以获得高达99%ee的含手性季碳桥联多环骨架。该方法将有效促进复杂天然产物的合成及新药研究(Angew. Chem. Int. Ed.2020, 59,8143-8147.)。

该研究工作得到国家自然科学基金委、中国科学院战略性先导科技专项(B类)、中国科学院、上海科委以及中国科学院上海有机化学研究所生命有机化学国家重点实验室的大力资助。