糖尿病、脂肪肝和肥胖症等代谢性疾病已经成为影响人类健康的一大“杀手”,研究显示一些孤儿受体可能成为治疗这些疾病的重要靶点。GPR119又被称为葡萄糖依赖的促胰岛素受体(Glucose-dependent insulinotropic receptor),是G蛋白偶联受体(GPCR)超家族中的一种孤儿受体。由于其在糖代谢调控中的作用,GPR119被认为是一种治疗糖尿病、脂肪肝和肥胖症等代谢性疾病的潜在药物靶点。GPR119主要分布在胰岛β细胞和胃肠道L细胞,调节葡萄糖依赖的促胰岛素的分泌。GPR119的激活可以刺激胰高血糖素样肽-1(GLP-1)和葡萄糖依赖性促胰岛素释放多肽(GIP)的分泌,这两种激素是调控体内糖代谢平衡的重要物质。
近年来,越来越多的GPR119小分子激动剂被开发,作为开发口服治疗糖尿病的临床药物。然而,由于对GPR119功能和激活机制理解的匮乏,限制了靶向GPR119的小分子药物的开发。因此对于此靶点更深入的分子水平研究成为该领域重要的研究热点,而揭示GPR119与内源性配体以及药物分子的相互作用机制也成重要的科学问题。此外,GPR119被一直认为有较高“自激活”活性,但这种“自激活”的原因和结构基础尚不明确。
2022年8月15日,国科大杭高院药物科学与技术学院(以下简称药学院)双聘教授谢欣研究员、中科院上海药物研究所徐华强研究员、联合临港实验室蒋轶研究员,在Nature Structural & Molecular Biology发表了最新的研究成果“Structural identification of lysophosphatidylcholines as activating ligands for orphan receptor GPR119”。研究发现,在不加任何外源配体的情况下,GPR119即能结合细胞膜中的溶血磷脂酰胆碱(lysophosphatidylcholines,LPC)并被其激活,完美解释了一些受体的所谓“自激活”现象其实是由未知内源配体导致。研究还解析了GPR119与临床阶段小分子候选药物APD668复合物的冷冻电镜结构,并阐明了受体偶联下游Gs信号蛋白的分子机制。
为了研究GPR119的结构,研究人员从昆虫细胞中表达纯化了人源GPR119受体和Gs蛋白三聚体的复合物样品,并在未加入小分子配体的情况下解析了GPR119与Gs蛋白的复合物结构,分辨率为3.1埃。通过结构观察,研究人员意外地发现受体的配体结合口袋存在一个狭长的小分子配体密度。为了鉴定该小分子的种类,研究人员将复合物样品进行质谱分析,结果表明该小分子密度属于具有单链疏水性尾部的溶血磷脂酰胆碱(LPC)。研究人员进一步在细胞水平验证了不同种类溶血磷脂对GPR119的激活作用,结果显示不同种类的溶血磷脂对GPR119均有不同程度的激活作用。
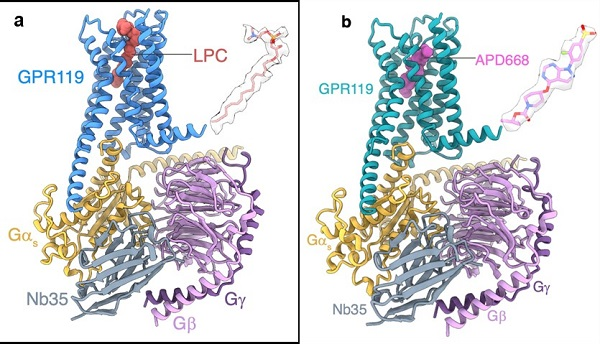
图1. GPR119/Gs与溶血磷脂酰胆碱(LPC)(a)或临床小分子候选药物APD668(b)复合物的冷冻电镜结构。
GPR119的配体结合口袋可以分为两部分:疏水和亲水口袋。其中疏水口袋贯穿于胞外区和受体中央位置,主要与LPC的疏水性尾部结合;而亲水口袋向胞外区延伸,主要与LPC的亲水性头部结合。值得注意的是,GPR119的口袋呈狭长状,在受体中央部位形成一个开口,使得配体结合口袋和细胞膜进行连通。而这个开口的形成与GPR119的跨膜螺旋5(TM5)独特的结构有关。在GPR119的TM5中间位置(5x50)附近,GPR119的氨基酸序列从结构上呈现出与其他Class A GPCR相比交错一位的特征,从而形成了独特的开口结构。此开口结构既为较长的单链磷脂提供了结合空间,同时也提供了另一个潜在的配体入口。借助分子对接的手段,研究人员提出了该开口附近可能构成别构调节剂的结合位点,并探讨了具有控制食欲作用的多糖类天然产物Gordonoside F与该别构位点的潜在结合方式。
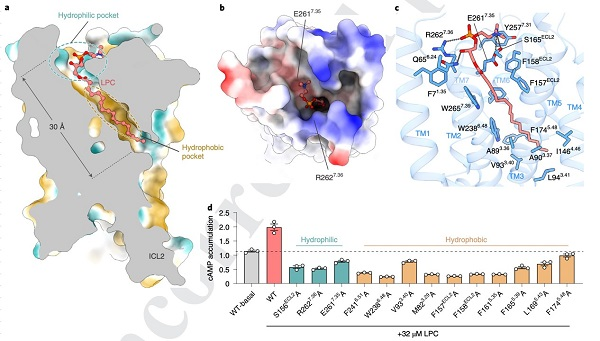
图2. LPC在GPR119中的结合口袋及关键氨基酸突变对受体活性的影响。
为了研究高亲和力配体、临床候选小分子药物与GPR119的结合机制,研究人员解析了代表性激动剂APD668与GPR119复合物的结构,分辨率为2.8埃。研究人员发现APD668较为刚性的结构骨架主要占据GPR119的疏水口袋,并且与该口袋中的氨基酸形成了更强的相互作用,提供配体较高的亲和力。此外,研究人员发现GPR119的激活开关(Toggle Switch)残基W2386.48呈现与其他受体不同的偏转方式,并且在该残基附近发现一个水分子与周围残基形成氢键,稳定了受体的激活构象。
综上,本研究首次报道孤儿受体GPR119偏好性结合LPC的分子机制,提出部分所谓具有“自激活”活性的受体可能是由于结合了未知配体而导致的观点;首次解析了GPR119与内源性配体LPC以及临床候选小分子药物APD668的结构,揭示了GPR119被小分子激活的结构基础;同时发现了GPR119独特的结构特征和潜在的别构调节剂的结合位点,为靶向GPR119的代谢性疾病药物开发提供了重要结构基础。
上海药物所徐沛雨博士(现为MIT博士后)、黄思婕博士(现为UCSF博士后)、上海药物所助理研究员郭世猛和国科大杭高院药学院博士后贠盈为本文共同第一作者。国科大杭高院药学院院长蒋华良院士、上海药物所周虎研究员也提供了大量协助工作。该工作得到科技部重点研发计划、国家自然科学基金委、上海市市级科技重大专项、中科院战略性先导科技专项等项目的资助。
DOI: 10.1038/s41594-022-00816-5
 国科大杭高院药学院
国科大杭高院药学院